Felix Vallejo López
Hospital Veterinario Happy Animal.
Tampico 34
MADRID
felix.vallejo@happyanimal.es
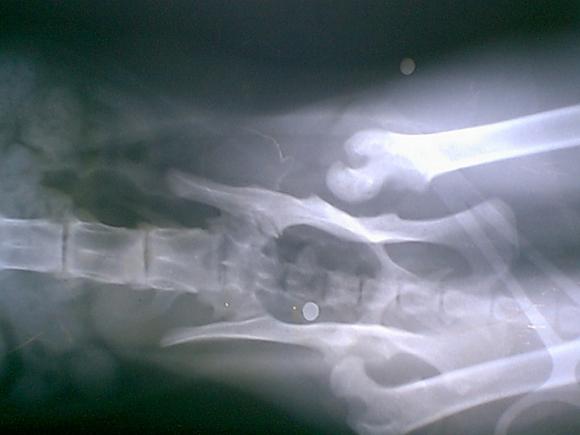
DISPLASIA DE CADERA
Es una enfermedad cada vez mas frecuente, y puede afectar a todas las razas de gato, pero especialmente tiene mayor incidencia en razas grandes como Main Coon. También se encuentra en Bosque de Noruega, Brithis, Ragdoll o persa.
Sabemos su origen genético pero no tenemos tipificado los genes implicados, intentamos emplear los modelos caninos para crear un paralelismo en la transmisión pero sin éxito, ni siquiera en el caso del perro lo hemos obtenido, sabemos que existen 16 pares de genes implicados, pero no se repite la misma sintomatología en animales idénticos genéticamente, por lo tanto deben existir otros genes modificadores de la expresión que no conocemos.
Otro problema al que nos enfrentamos, es la variación de tamaño entre diferentes razas felinas, en 1990 en un trabajo realizado en la Universidad de Wien (Austria) por Koppel E y Ebner J. Se realizaron mediciones del ángulo de Norber-Olsson en 293 gatos normales y con DC. Los autores proponen que ángulos menores de 95 º son indicativos de displasia, como vemos nos basamos en trabajos estadísticos, sobre poblaciones de gatos.
El ángulo de Norber- Olsson es el ángulo que se forma entre una línea que une cada centro de las cabezas femorales con los respectivos bordes craneales de sus acetábulos y otra línea que pasa por el centro de ambas cabezas.
Dentro del mismo estudio se vio que dentro de los gatos de raza Main Coon , la penetración de la enfermedad llegaba al 18 % de los gatos explorados, y en otros estudios sobre poblaciones que superan los 200 animales la incidencia para esta raza estaba en torno al 24 %.
Los síntomas mas frecuentes son dolor al saltar, reticencias a ser cogidos en brazos y cojeras y claudicaciones evidentes.
En ocasiones se aprecia luxación de rotula bilateral quizás debido al cambio en la linea longitudinal del aplomo del animal, y al mismo tiempo pueden aparecer compromisos neurológicos en la columna lumbar debido al cambio en la postura al andar.
¿POR QUE ALGUNOS GATOS DISPLÁSICOS TIENEN SINTOMAS Y OTROS NO?
Exploraciones en familias completas de gatos nos muestran que no hay relación directa entre dolor y signos radiológicos, animales con pequeñas lesiones en las placas a veces muestran dolores severos y viceversa. En la dedada de los 90, el diagnostico radiológico significaba el 90 % del diagnostico de la displasia (perros) ahora damos una importancia capital a la exploración de la articulación temprana, animales de menos de un año con inestabilidad articular (signo de Ortolani positivo) son altamente sugestivos de padecer displacía de cadera.
Del mismo modo no podemos olvidar que la información genética para la expresión de un carácter ( GENOTIPO) se complementa con los factores Displasia felina con luxacion e inestabilidad completa de ambas articulaciones que modelan dicho carácter ( FENOTIPO) , y de la complementacion de ambos surge la expresión final que es lo que nosotros vemos.
No podemos actuar sobre el GENOTIPO, pero si sobre el FENOTIPO. Los últimos estudios en perros nos muestran una relación entre energía y proteína en la alimentación y signos de displasia en el animal adulto, de modo que debemos mantener a nuestros animales en un peso muy correcto y no promover una musculación excesiva, el desarrollo del músculo pectineo de modo temprano se asocia a cuadros de dolor tempranos. Todos estos estudios se han desarrollados en perros, y se esta trabajando para extrapolarlos en nuestro paciente felino.
Los SINTOMAS en el gato son menos evidentes que en el perro ¿Por qué?
El gato tiene menos peso que el perro y sospechamos que esa es una de las causas mas pausibles, ademas de tener un esqueleto mas ligero. El gato es ademas un animal que no sale a pasear con correa que promueve ejercicios y esfuerzos de carga. Un gato con dolor en un domicilio no se mueve, es mas sedentario que el perro.
HCM
La Cardiomiopatia hipertrofica se define como la hipertrofia del ventriculo izquierdo en ausencia de otras causas sistémicas que lo produzcan de modo secundario. Puede ser focal o generalizada. Se ha descrito en Main Coon, Ragdolls, Persas y American Short Hairs. Se afecta la producción de beta-miosina que forma parte del músculo cardiaco. En algunas ocasiones se relaciona este proceso con el aumento de la hormona de crecimiento. Se sabe del mismo modo que los mecanismos de la regulación del calcio están alterados en el músculo cardiaco.
Los signos clínicos son amplios como murmullos, ritmos de galope, y según va avanzando el proceso encontramos disnea, arritmias y debido al reflujo provocado en el atrio cardiaco podemos tener troembolismos que cursan con parálisis y/o parexia de algún miembro, pudiendo cursar incluso con la muerte del animal.
La cardiomiopatia hipertrófica en el gato es una patología bien descrita a nivel clínico, sabemos como se desarrolla la enfermedad y podemos instaurar los tratamientos de mantenimiento correcto para asegurarnos una correcta calidad de vida en nuestro paciente, no obstante sabemos que en algunos casos tiene una base genética , aislándose dos mutaciones diferentes, que afectan al mismo gen en diferentes razas especialmente Main Coon, y Ragdolls.
La mutación específica para HCM en los gatos de raza Ragdoll produce síntomas tempranos de la enfermedad con una edad media en la diagnosis de 15 meses. También parece que los animales homocigoticos (2 copias) para la mutación tienen una edad anterior del inicio de la enfermedad que los heterocigoticos (1 copia). La mutación, conocida como R820W, es un solo cambio en el gen MYBPC3 que altera la forma y la función de la proteína esencial para el desarrollo normal del miocardio. La misma mutación de R820W se ha encontrado recientemente para ser asociada a HCM y a la no-compactación ventricular izquierda en seres humana (Ripoll y otros. 2010), con lo cual se aplican con vistas al futuro los mismos modelos de estudio laboratorial para el estudio de la enfermedad que en medicina humana.
Es muy importante saber que la falta de la mutación en un gato no significa que nunca desarrollará la enfermedad. Esto significa que no tiene la única mutación conocida que puede causar la enfermedad en el gato en este momento. En el futuro, se pueden identificar mutaciones adicionales que puedan probar los casos que actualmente son negativos para estas mutaciones pero que acaban desarrollando la enfermedad.
Existen dos pruebas independientes para ambas mutaciones; y son la prueba para la mutación que se encuentran predominantemente en Maine Coons, y la otra prueba es para la mutación que predominantemente se encuentra en Ragdolls. En la actualidad se esta trabajando en la puesta a punto de una prueba especifica para Bosque de Noruega
Si un gato es negativo: Esto significa que el gato no tiene la mutación. Este animal no desarrollara HCM provocada por esta mutación genética, pero podría desarrollar enfermedades del corazón durante su vida. Si un gato es positivo para la mutación de HCM: Esto significa que el gato tiene la mutación de cardiomiopatía hipertrófica y es muy probable que se desarrolle la enfermedad en un futuro.
PKD
Poliquistosis renal (enfermedad de riñón poliquístico) es una anomalía bien documentada en gatos domésticos. Los riñones poliquísticos esporádicamente pueden aparecer en cualquier población de gatos. Poliquistosis renal no es una enfermedad nueva y se ha reportado en la literatura durante más de 30 años. La forma hereditaria de PKD puede haber ocurrido inicialmente en persas como una mutación, y sabemos que en su origen tienen que ver con la raza persa y todas las razas en las que ha participado esta en su evolución. La PKD no tiene una fuerte presentación clínica lo cual ha provocado que durante muchos años de modo silente haya avanzado a nivel genético en esta raza ya que la variabilidad de los cuadros clínicos y el hecho de que diera signos en animales de edad avanzada hacia que no se detectara de modo temprano, y no se pudiera prevenir a nivel reproductor. Los avances en diagnostico por imagen hace una década empezaron a permitir planificar buenos planes reproductivos en algunos criaderos.
La casuística de PKD dentro de la enfermedad renal es similar a otras causas comunes de muerte para cualquier gato con insuficiencia renal. Así, el PKD ha pasado inadvertida durante muchos años y se ha extendido a lo largo de la raza persa. Cualquier raza que ha usado a persas en su fundación o propagación debería tener controlado genéticamente su población para esta enfermedad.
En persas, la condición ha demostrado ser heredada como un solo gen autosómico dominante. Se estima que más del 37% de los persas tienen PKD, una raza que representa casi el 80% de la población felina a nivel de raza en algunos paises (Davis 2009) Otros autores llegan a cifrarlo en el 45 % de la población de persas (Jacquie Rand 2006). Muchas líneas y criaderos han sido capaces de reducir en gran medida la incidencia de la enfermedad mediante el uso de métodos de detección (tanto laboratoriales y de ultrasonido) y mejorando las prácticas de cría.
La presentación de la enfermedad es más común en los persas y razas que están relacionadas con los ellos( exóticos, British shorthair y Scottish Fold), aunque también lo encontramos en gatos comunes europeos.
Es una enfermedad de aparición precoz a nivel anatómico con presentación bilateral (ambos riñones) y múltiples quistes son característicos de la enfermedad. Los quistes se presentan temprano, a menudo antes de 12 meses de edad. Sin embargo, insuficiencia renal, generalmente ocurre a una edad tardía, por lo tanto puede pasar desapercibida
Al ser una enfermedad autosómica dominante implica que solo una copia del gen se requiere para producir PKD de modo que el 50% de la descendencia de los gatos positivos a PKD heredará PKD.
Un gato positivo podría ser potencialmente homocigoto(es decir tener las dos cadenas de su ADN con el gen mutado, habiéndolo recibido tanto de su madre como de su padre) y todos los descendientes producidos tendría PKD, pero es infrecuente ya que se sospecha que la condición de homocigoto para PKD podría ser letal en el útero o presentar un cuadro clínico muy severo a una edad muy temprana y provocar la muerte del cachorro. Se requiere más investigación para probar los efectos de la condición de homocigoto.
¿Qué gatos deben someterse a pruebas para PKD? Actualmente se recomienda la prueba PKD para British Shorthair, persas, exóticas y Scottish Fold.
GSD IV
GSD IV (almacenamiento de glucógeno tipo IV) es un trastorno hereditario que afecta al metabolismo de la glucosa. Esta deficiencia hereditaria que se conoce en humanos, caballos y gatos (bosque de noruega)
Los gatitos afectados nacen muertos o mueren poco después del nacimiento, presumiblemente debido a la hipoglucemia ( ya que no son capaces de producir suficiente cantidad de glucosa «energía») durante el proceso de nacimiento y las primeras horas de vida. En casos muy raros los cachorros afectados pueden vivir hasta 4-5 meses de edad, presentando debilidad fiebre en agujas, temblores y ataxia.
En estos casos el crecimiento se detiene y la enfermedad conduce a la degeneración neuromuscular progresiva, a la debilidad muscular intensa, las contracciones, la atrofia y la imposibilidad de usar sus extremidades (sobre todo las patas traseras) son los signos mas evidentes. La muerte se suele producir antes de los 15 meses.
El gen responsable de la enfermedad ha sido identificado por el Dr. John Fyfe en los EE.UU., que también desarrolló una prueba genética para la mutación en gatos Bosques de Noruega en 1996. En Europa, esta prueba ha estado disponible desde 2007. La prevalencia de la enfermedad reportada es alrededor del 15% en los EE.UU., mientras que las estadísticas en Europa son de un 12%.
GSD IV se hereda como un proceso autosómicos recesivo, lo que significa que ambos padres deben ser portadores del gen mutado para producir descendencia afectada.
SMA (ATROFIA MUSCULAR ESPINAL DEL MAIN COON)
SMA es un trastorno hereditario que afecta a los músculos del esqueleto del tronco y las extremidades. La pérdida de neuronas en los primeros meses de la vida conduce a la debilidad muscular y atrofia haciéndose evidente a los 3-4 meses de edad. Los gatitos afectados desarrollan un modo extraño de andar con un balanceo de los cuartos traseros y los tarsos casi tocando el suelo. A los 5-6 meses de edad son incapaces de saltar en altura. La atrofia muscular es evidente. No hay dolor.
Pueden ser animales que pueden convivir con los demás sin demasiado problema, pueden tener alteraciones o crisis de la enfermedad avanzando la atrofia muscular, pero el máximo avance del proceso se produce en el periodo juvenil.
No presentan incontinencia pero si intolerancia al ejercicio y en algunos casos asociada a disnea de esfuerzo.
Este trastorno se hereda con un gen autosómico recesivo. Ambos padres deben transmitir la enfermedad, machos y hembras se ven afectados por igual. Los padres de los gatitos afectados no muestran signos externos de la enfermedad, pero son portadores en muchos casos.
Enfermedades del deposito lisosomial (GM2) en gatos birmanos
La GM2 gangliosidosis es una enfermedad hereditaria conocida como enfermedad de depósito lisosomal «, llamados así porque se caracteriza por la acumulación de material sin procesar en los lisosomas agrandados. Carecen de las enzimas que eliminan los procesos de desecho celular. Los productos de desecho se acumulan dentro de la propia célula. Las células afectadas son las neuronas por lo tanto, los síntomas son neurologicos. Los síntomas aparecen por primera vez alrededor de los 6 a 8 semanas de edad.
El comienzo de la enfermedad es un temblor que aumenta de modo intencional. Esta es una enfermedad progresiva y fatal, y estos temblores se hará más pronunciados a medida que el gatito crezca. Cuando el gato está en reposo, los temblores son menos obvios.
A medida que avanza la enfermedad, y los temblores se hacen más intensos, el gatito se pasara más tiempo en reposo. Los síntomas son graves en torno a los 4 meses.
Esta enfermedad es una enfermedad autosómica recesiva y se manifiesta sólo cuando ambos padres son portadores del gen.
Hay una prueba de ADN disponible que detectará la presencia del gen GM2. Fue desarrollado por el Dr. Henry Baker, del Centro de Investigación Scott-Ritchey en el Colegio de la Universidad de Auburn de Medicina Veterinaria.
Deficiencia en Piruvato kinasa (PK)
Piruvato quinasa (PK) es una enzima esencial para la vía anaeróbica glicolítica de la producción de energía en el eritrocito. Si los eritrocitos son deficientes en PK son incapaces de mantener el metabolismo normal de la célula y por lo tanto se destruyen prematuramente. Esta deficiencia se manifiesta como una anemia hemolítica de intensidad variable.
Deficiencia de PK se hereda como un trastorno autosómico recesivo. Los portadores con un gen normal y uno defectuoso de la piruvato quinasa no tienen ningún signo clínico de la enfermedad y llevan una vida normal. Sin embargo, cuando se utiliza en la cría de ellos son capaces de propagarse mutaciones en la población.
Deficiencia de PK han sido reconocidos tanto en perros y gatos.
En los gatos, la deficiencia de PK se ha descrito en gatos abisinios y somalíes, en USA también se ha referido en otras razas.
Para los perros de la deficiencia en última instancia conduce a síntomas severos como osteoporosis y la insuficiencia hepática y la esperanza de vida se reduce a los cuatro años. En contraste, la anemia en los gatos puede ser intermitente con hematocrito normal en valores medios y los gatos afectados no parecen desarrollar síntomas hepáticos u oseos.
Los síntomas de la anemia a menudo se acompañan de intolerancia al ejercicio y esplenomegalia.
La esperanza de vida de los gatos con esta enfermedad es variable, pudiendo ser normal o morir a los dos años de vida.
Deficiencia de PK se pueden detectar con pruebas de ADN.
ATROFIA RETINIANA PROGRESIVA (PRA)
La atrofia progresiva de retina se hereda como una enfermedad autosómica recesiva simple en la mayoría de las razas. PRA ha sido reconocido en los seres humanos, en la mayoría de perros de raza pura y algunas razas de gatos.
La retina contiene células especializadas llamadas fotoreceptores. Estos absorben la luz enfocada sobre ellos por el cristalino del ojo, y convierten la luz en señales nerviosas eléctricas. Las señales nerviosas se transmiten por el nervio óptico hasta el cerebro donde se percibe como la visión. En la ARP en los gatos abisinios y somalíes, los fotorreceptores degeneran poco a poco.
La visión nocturna es lo primero en deteriorarse a medida que el gato se enfrentará a mayores problemas de ajuste de su visión a la luz tenue. Después afectará a la visión diurna.
Cursa con hiperreflexia y dilatación pupilar.
La Ceguera total se produce normalmente en torno a los 4-5 años, pero podría retrasarse por varios años.
El diagnostico oftalmologico es sencillo, pero lo ideal es saber de modo temprano para poder incluirlo o no en los programa de cria. Si existe una prueba genetica de diagnostico,
Bibliografia:
1.- Problem-based in Feline Medicine : Jacquie Rand, Ed Saunder Elsevier 2006.
2.- Tratado de Medicina Interna Veterinaria Sexta edición: S. Ettinger , E. Feldman, Ed. Elsevier Saunder 2007.
3.- El paciente felino, Tercera Edición. G. Norsworthy, M. Crystal. Ed. Interamericana. 2009
4.- Medicina Cardiovascular de pequeños animales, M. Kitttleson, R. Kienle. Ed. Mosby 2000.
5.- Koppel E.; Ebner J. Dysplasia of the hip joint in cat. Kleintierpraxis 35-6 . 1990.
6.- Patsikas M.N.;Papazoglou L.G.;Komninou A.;Dessiris A.K.; Tsimopoulos G. Hip dysplasia in the cat: a report of three cases .(Greece) Journal of Smal-Animal Practice 39-6. 1998.